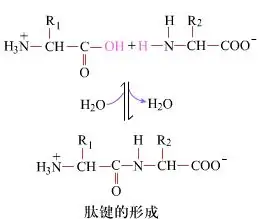
Na powierzchni tworzenie wiązań peptydowych, w wyniku których powstają dipeptydy, jest prostym procesem chemicznym.Oznacza to, że dwa składniki aminokwasowe są połączone wiązaniem peptydowym, wiązaniem amidowym, podczas gdy są odwodnione.
Tworzenie wiązania peptydowego polega na aktywacji aminokwasu w łagodnych warunkach reakcji.(A) ugrupowanie karboksylowe, drugi aminokwas. (B) Nukleofilowo aktywowane ugrupowanie karboksylowe tworzy następnie dipeptyd (AB).„Jeśli składnik karboksylowy (A) nie jest chroniony, nie można kontrolować tworzenia wiązania peptydowego.”Produkty uboczne, takie jak peptydy liniowe i cykliczne, można mieszać ze związkami docelowymi AB.Dlatego wszystkie grupy funkcyjne nie biorące udziału w tworzeniu wiązań peptydowych muszą być chronione w sposób tymczasowo odwracalny podczas syntezy peptydu.
Zatem synteza peptydów – tworzenie każdego wiązania peptydowego – obejmuje trzy etapy agregacji.
Pierwszym krokiem jest przygotowanie niektórych aminokwasów, które wymagają ochrony, a obojnacza struktura aminokwasów już nie istnieje.
Drugi etap to dwuetapowa reakcja tworzenia wiązań peptydowych, w której grupa karboksylowa N-zabezpieczonego aminokwasu jest najpierw aktywowana do aktywnego związku pośredniego, a następnie tworzy się wiązanie peptydowe.Ta sprzężona reakcja może przebiegać jako reakcja jednoetapowa lub jako dwie kolejne reakcje.
Trzecim krokiem jest selektywne usunięcie lub całkowite usunięcie podstawy ochronnej.Chociaż całkowite usunięcie może nastąpić dopiero po złożeniu wszystkich łańcuchów peptydowych, w celu kontynuacji syntezy peptydów wymagane jest również selektywne usunięcie grup ochronnych.
Ponieważ 10 aminokwasów (Ser, Thr, Tyr, Asp, Glu, Lys, Arg, His, Sec i Cys) zawiera grupy funkcyjne łańcucha bocznego, które wymagają selektywnej ochrony, co komplikuje syntezę peptydów.Należy rozróżnić tymczasowe i półstałe podstawy zabezpieczające ze względu na różne wymagania dotyczące selektywności.Tymczasowe grupy zabezpieczające stosuje się w następnym etapie, aby odzwierciedlić tymczasowe zabezpieczenie aminokwasów lub karboksylowych grup funkcyjnych.Półtrwałe grupy zabezpieczające są usuwane bez zakłócania już utworzonych wiązań peptydowych lub łańcuchów bocznych aminokwasów, czasami podczas syntezy.
„W idealnym przypadku aktywacja składnika karboksylowego i późniejsze tworzenie wiązań peptydowych (reakcje sprzęgania) powinny być szybkie, bez tworzenia się racemii lub produktów ubocznych, a w celu uzyskania wysokiej wydajności należy zastosować reagenty molowe”.Niestety, żadna z metod sprzęgania chemicznego nie spełnia tych wymagań, a niewiele z nich nadaje się do praktycznej syntezy.
Podczas syntezy peptydów grupy funkcyjne biorące udział w różnych reakcjach są zwykle połączone z centrum ręcznym (wyjątkiem jest glicyna) i istnieje potencjalne ryzyko rotacji.
Ostatnim etapem cyklu syntezy peptydów jest usunięcie wszystkich grup ochronnych.Selektywne usuwanie grup ochronnych jest ważne dla wydłużania łańcucha peptydowego, oprócz wymogu całkowitego usunięcia zabezpieczeń w syntezie dipeptydów.Strategie syntetyczne należy dokładnie zaplanować.W zależności od wyboru strategicznego N może selektywnie usuwać grupy zabezpieczające α-aminowe lub karboksylowe.Termin „strategia” odnosi się do sekwencji reakcji kondensacji poszczególnych aminokwasów.Ogólnie rzecz biorąc, istnieje różnica między stopniową syntezą a kondensacją fragmentów.Synteza peptydów (znana również jako „synteza konwencjonalna”) odbywa się w roztworze.W większości przypadków stopniowe wydłużanie łańcucha peptydowego można zsyntetyzować jedynie poprzez wykorzystanie łańcucha peptydowego do syntezy krótszych fragmentów.Aby zsyntetyzować dłuższe peptydy, cząsteczki docelowe należy podzielić na odpowiednie fragmenty i ustalić, czy mogą zminimalizować stopień zróżnicowania na C-końcu.Po stopniowym łączeniu poszczególnych fragmentów docelowy związek zostanie połączony.Strategia syntezy peptydów obejmuje wybór najlepszego i najbardziej odpowiedniego fragmentu zabezpieczającego, natomiast strategia syntezy peptydów obejmuje wybór najodpowiedniejszej kombinacji zasad ochronnych i najlepszej metody koniugacji fragmentów.
Czas publikacji: 19 lipca 2023 r