Technologia syntezy podobna do peptydu
Badania i rozwój leków peptydowych szybko rośnie w medycynie. Jednak rozwój leków peptydowych jest ograniczony własnymi cechami. Na przykład, ze względu na specjalną wrażliwość na hydrolizę enzymatyczną, stabilność jest zmniejszona, a zmienność konformacji sterycznej powoduje niską specyficzność ukierunkowaną, niską hydrofobowość i brak określonego systemu transportu. Aby przezwyciężyć te peptydy, jeden z nich zaproponował wiele rozwiązań i pomyślne zastosowanie jednego rodzaju peptydu.
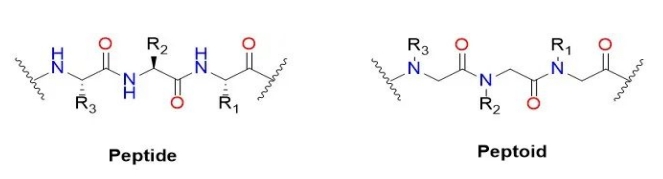
Rodzaj peptydu (nazwa angielskiego: peptoid) lub poli - n - zamiast glicyny (nazwa angielskiego: Poly Real - N - podstawa jest to quasi peptydowe związki peptydu w łańcuchu głównym. Łańcuch boczny węglowego alfa przenosi azot głównego łańcucha zamiast łańcucha bocznego. W oryginalnym polipeptydu grupa R łańcucha bocznego aminokwasów reprezentuje 20 różnych aminokwasów, ale grupa R ma więcej opcji w peptoidach. W peptydzie peptyd na głównym łańcuchu aminokwasów w azotu węglowym alfa zamiast przenoszenia łańcucha bocznego do łańcucha głównego. Warto wspomnieć, że ogólnie peptydy nie wytwarzają takich samych uporządkowanych struktur, jak struktury wtórne w peptydach i białkach z powodu braku wodoru w azotu szkieletowym. Peptydem początkowym celem jest opracowanie stabilnego i proteazy peptydu leków małych cząsteczek.
Analiza technik syntezy podobnych do peptydu
Wprowadzono metodę syntezy peptydów
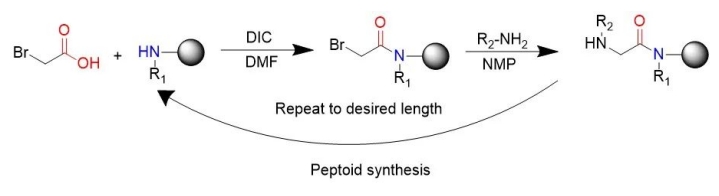
Ogólnie popularną metodą syntezy podobną do peptydu jest metoda syntezy podsumowej wymyślona przez Ronzuckermanna, z których każda jest podzielona na dwa etapy: acylowanie i przemieszczenie. W acylacji pierwszym krokiem jest aktywacja kwasu halooctowego w celu reakcji z aminami pozostającymi na końcu poprzedniego kroku, najczęściej diiisopropylowalizowanej dieiminy. Bromoaceciecid był aktywowany przez diizopropylokarbodiimid. „W reakcjach podstawienia (bimolekularne reakcje podstawienia nukleofilowe) amina, zazwyczaj pierwotna, atakuje alternatywny halogen z utworzeniem glicyny podstawionej N.” Subunitarna syntetyczna trasa wykorzystuje łatwo dostępne pierwotne aminy do generowania peptydów, umożliwiając w ten sposób chemiczną syntezę peptydów.
Solidne rozszerzenie w syntezie peptydów klasowych ma bogate doświadczenie, może zapewnić różnorodne usługi syntezy peptydów.
Analiza technik syntezy podobnych do peptydu
Zaleta takiego peptydu
Bardziej stabilne: peptoidy są bardziej stabilne in vivo niż peptydy.
Więcej selektywności: peptoidy dobrze nadają się do połączonych badań odkrywania leków, ponieważ wiele różnych bloków konstrukcyjnych polipeptydowych można uzyskać przez modyfikację grupy aminowej szkieletu.
Bardziej wydajne: obfitość struktur peptoidów może uczynić peptoid dobrym wyborem dla metodologii skanowania w celu szybkiego znalezienia określonych struktur wiążących się z białkami.
Większy potencjał rynkowy: Charakterystyka tego rodzaju peptydu niech stała się rodzajem rozwoju leku, ma ogromny potencjał.
Czas postu: 2025-07-02